La resistencia antimicrobiana (AMR) es una de las mayores amenazas para la salud pública a nivel mundial y una prioridad estratégica en España.
Este artículo destaca la importancia comprender cómo ciertos desinfectantes —y su modo de acción— pueden influir en este fenómeno es fundamental para garantizar la seguridad del paciente, del profesional sanitario y del propio sistema sanitario.
Descubre cómo soluciones innovadoras, como los desinfectantes esporicidas y de alto nivel basados en dióxido de cloro de Tristel, pueden ofrecer una defensa fiable frente a la AMR, garantizando una desinfección responsable sin contribuir a esta creciente amenaza para la salud pública.
Nos enfrentamos a una emergencia sanitaria…
La resistencia antimicrobiana es un problema mundial de salud pública. En 2019, causó directamente más de 1,27 millones de muertes y contribuyó a otras 4,95 millones. Además de su impacto en la salud, la AMR supone una carga económica significativa: sin cambios, los costes sanitarios y las pérdidas de productividad podrían alcanzar hasta 1 billón de dólares en 2050.¹
Sin intervenciones efectivas, corremos el riesgo de entrar en una era posantibiótica, en la que infecciones comunes —antes tratables— podrían convertirse en cuadros graves o incluso intratables.

Los antibióticos: una de las causas de las resistencia antimicrobiana
El uso inadecuado de antibióticos es una de las principales causas del aumento de la resistencia antimicrobiana. En España, el PRAN identifica tres prácticas especialmente relevantes: la prescripción excesiva, el uso inapropiado y la interrupción prematura de los tratamientos. Cada una de ellas contribuye a que determinados microorganismos sobrevivan y desarrollen mecanismos de defensa frente a los antibióticos.
Pero los antibióticos no son los únicos: algunos biocidas también están bajo revisión
Los antibióticos no son los únicos implicados en la resistencia antimicrobiana. Diversos estudios y organismos internacionales han señalado que ciertos biocidas utilizados en la desinfección de dispositivos médicos y superficies podrían desempeñar un papel en el desarrollo de tolerancia microbiana, especialmente cuando se emplean de forma inadecuada.
Entre ellos, los compuestos de amonio cuaternario (QACs) son los que concentran mayor atención. Estos agentes son tensioactivos de carga positiva con actividad frente a un espectro limitado de microorganismos —bacterias, levaduras y virus envueltos—, actuando principalmente sobre la membrana celular.²
En condiciones óptimas, los QACs pueden desestabilizar la membrana hasta provocar su ruptura. Sin embargo, este efecto no se produce a cualquier concentración ni en todos los escenarios. Cuando las concentraciones son bajas o los tiempos de exposición no son los adecuados, los QACs pueden interactuar con microorganismos tolerantes sin llegar a eliminarlos.

En términos sencillos, los QACs penetran en los microorganismos para provocar su muerte. Esta alteración no ocurre de forma inmediata ni a cualquier concentración. En muchos casos, solo se produce cuando se emplean altas concentraciones de QACs o combinaciones de QACs.
En todos los demás casos, los QACs pueden interactuar con microorganismos tolerantes, pero no hasta el punto de provocar su muerte.
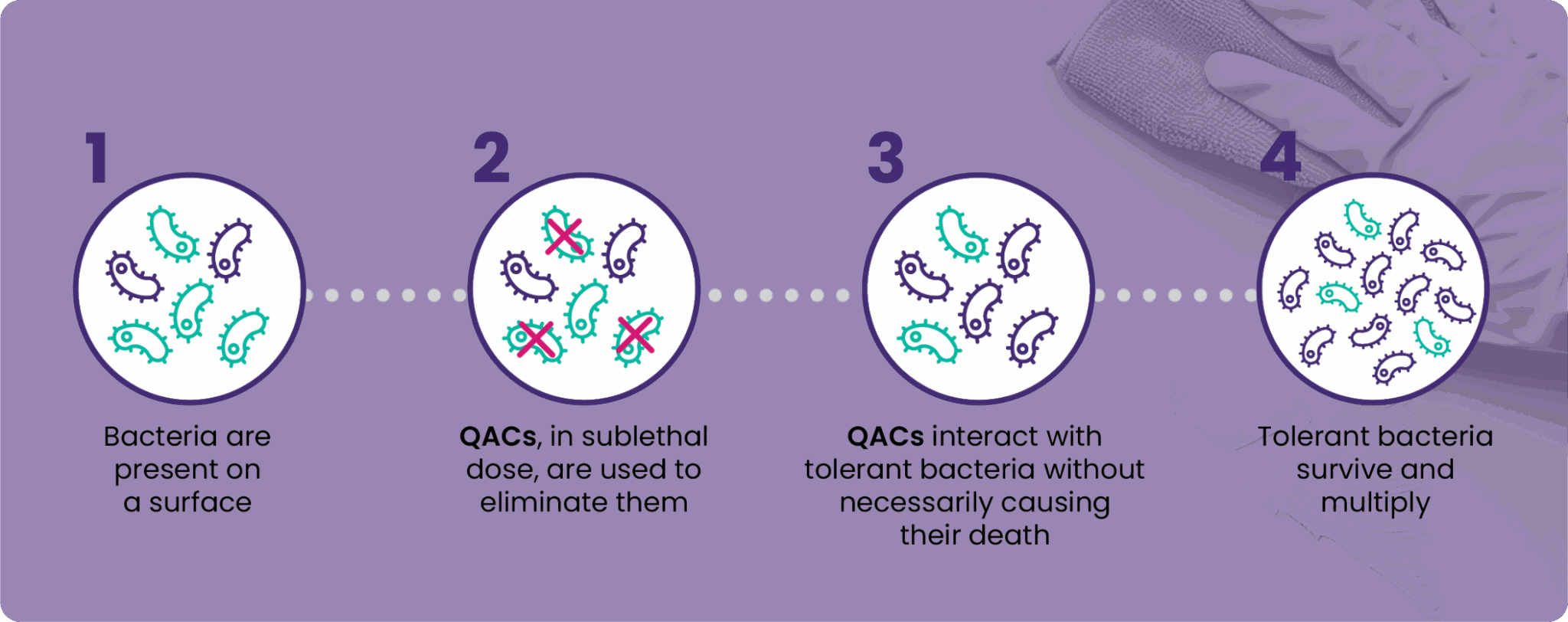
Es en esta zona gris donde la resistencia antimicrobiana (AMR) se convierte en una amenaza real que debe ser vigilada de cerca.
Cuando un microorganismo sobrevive a una concentración subletal de un biocida, puede desarrollar tolerancia, un fenómeno conocido como resistencia bacteriana adquirida.
A nivel genético, el microorganismo puede desarrollar estructuras llamadas bombas de eflujo, que permiten a la célula regular su entorno interno expulsando activamente los agentes desinfectantes que penetran en ella. Esto reduce su efecto tóxico y ayuda a los microorganismos a sobrevivir en un entorno con dosis subletales de desinfectantes.

Esta resistencia bacteriana adquirida no se limita a un solo microorganismo. Las bacterias que han aprendido a defenderse transmitirán su gen de resistencia a su descendencia o a bacterias cercanas mediante el contacto directo con otros microorganismos de la misma o de distinta especie.³
¿Cuál es la relación entre la tolerancia a los desinfectantes y la resistencia a los antibióticos?
Un microorganismo que ha adquirido resistencia frente a un determinado agente desinfectante puede utilizar mecanismos similares para resistir otros antimicrobianos, incluidos los antibióticos.⁴ A esto se le denomina co-resistencia o resistencia cruzada.
Por lo tanto, si un microorganismo que antes se eliminaba fácilmente con un espray o una toallita desinfectante deja de ser eliminado, el riesgo de que sobreviva e infecte a una persona aumenta considerablemente. Si ese mismo microorganismo utiliza sus mecanismos de resistencia adquirida para contrarrestar el efecto de un antibiótico, entonces corremos el riesgo de entrar en una era en la que las infecciones comunes podrían volverse imposibles de tratar.
Para el Sistema Nacional de Salud (SNS), este escenario supone un desafío importante: los desinfectantes que históricamente habían ofrecido protección pueden, si se utilizan de forma incorrecta o en concentraciones inadecuadas, contribuir sin querer al desarrollo y diseminación de la resistencia antimicrobiana.
Comprender cómo ciertos desinfectantes —y su modo de acción— pueden influir en este fenómeno es fundamental para garantizar la seguridad del paciente, del profesional sanitario y del propio sistema sanitario.
¿Qué podemos hacer para prevenir la resistencia a los antibióticos y la tolerancia a los desinfectantes?

En primer lugar, es importante limitar las dosis subinhibitorias, es decir, aquellas que no son lo suficientemente potentes para lograr el efecto deseado. Estas dosis bajas eliminarán solo a una parte de los microorganismos, pero los que sobrevivan serán menos sensibles a los antimicrobianos utilizados.5,6,7 Si este proceso continúa, la concentración activa de los antimicrobianos puede llegar a ser ineficaz.
En el caso de los biocidas utilizados para la desinfección de superficies, las soluciones con diluciones variables son especialmente problemáticas. No permiten tener la certeza de haber seleccionado la concentración adecuada, es decir, una concentración suficientemente potente y eficaz frente a todos los microorganismos potencialmente presentes en una superficie determinada.

En segundo lugar, deben evitarse los desinfectantes con tiempos de contacto variables y prolongados. Un tiempo de contacto largo con un biocida de baja reactividad química expone a los microorganismos a concentraciones subletales. Esto favorece la supervivencia de microorganismos infecciosos cuya susceptibilidad a los antimicrobianos se reduce.
Para evitar el riesgo de resistencia, es preferible utilizar soluciones con una única concentración, eficacia demostrada frente a todo el espectro de microorganismos y un tiempo de contacto corto y uniforme.
A diferencia de los QACs, la capacidad del ClO₂ de Tristel para eliminar un espectro completo de microorganismos está ampliamente demostrada, sin necesidad de ajustar la concentración por parte del usuario y sin tiempos de contacto variables o prolongados. La eliminación es casi inmediata (entre 30 segundos y 5 minutos según el producto) y se consigue con una única concentración (entre 100 ppm y 200 ppm dependiendo del producto).
¿Es adecuado utilizar desinfectantes de alto nivel para prevenir la resistencia antimicrobiana?
En el ámbito de la desinfección hospitalaria, resulta fundamental contar con agentes cuyo modo de acción sea estable, reproducible y eficaz frente a un amplio espectro de microorganismos. Entre las opciones disponibles, los desinfectantes de alto nivel basados en dióxido de cloro (ClO₂) destacan por su capacidad para actuar de manera efectiva sobre bacterias, virus, protozoos, levaduras, hongos, micobacterias y esporas.
El ClO₂ es un oxidante que elimina patógenos mediante el intercambio de electrones, sustrayéndolos de las estructuras vitales del microorganismo, como las paredes y membranas celulares, los orgánulos y el material genético. Es este intercambio el que provoca un desequilibrio molecular que conduce a la muerte segura del microorganismo.
Al tratarse de un agente concentración-estable y con tiempos de contacto uniformes, su rendimiento no depende de ajustes manuales ni de variaciones en la exposición. Esta consistencia facilita la estandarización del proceso de desinfección y contribuye al cumplimiento de los protocolos de los servicios de Medicina Preventiva y Control de Infecciones.8,9
References:
1 World Health Organization. (2023, November 21). Antimicrobial resistance. WHO. Retrieved August 16, 2024, from https://www.who.int/news-room/fact-sheets/detail/antimicrobial-resistance
2 Boyce, J. M. (2023). Quaternary ammonium disinfectants and antiseptics: Tolerance, resistance, and potential impact on antibiotic resistance. Antimicrobial Resistance & Infection Control, 12(32). https://doi.org/10.1186/s13756-023-01241-z
3 Vega, N. M., & Gore, J. (2014). Collective antibiotic resistance: Mechanisms and implications. Current Opinion in Microbiology, 21, 28-34. https://doi.org/10.1016/j.mib.2014.09.003
4 Ortega Morente, E., Fernández-Fuentes, M. A., Grande Burgos, M. J., Abriouel, H., Pérez Pulido, R., & Gálvez, A. (2013). Biocide tolerance in bacteria. International Journal of Food Microbiology, 162(1), 13-25. https://doi.org/10.1016/j.ijfoodmicro.2012.12.028
5 Walsh, S. E., Maillard, J. Y., Russell, A. D., Catrenich, C. E., Charbonneau, D. L., & Bartolo, R. G. (2003). Development of bacterial resistance to several biocides and effects on antibiotic susceptibility. Journal of Hospital Infection, 55(2), 98-107.
6 Voumard, M., Venturelli, L., Borgatta, M., et al. (2020). Adaptation of Pseudomonas aeruginosa to constant sub-inhibitory concentrations of quaternary ammonium compounds. Environmental Science: Water Research & Technology, 6(4), 1139-1152.
7 Soumet, C., Meheust, D., Pissavin, C., et al. (2016). Reduced susceptibilities to biocides and resistance to antibiotics in food-associated bacteria following exposure to quaternary ammonium compounds. Journal of Applied Microbiology, 121(5), 1275-1281.
8 Noszticzius, Z., Wittmann, M., Kály-Kullai, K., Beregvári, Z., Kiss, I., Rosivall, L. and Szegedi, J. (2013). Chlorine Dioxide Is a Size-Selective Antimicrobial Agent. PLoS ONE, 8(11), p.e79157. https://doi.org/10.1371/journal.pone.0079157
9 Block, S., Knapp, J., & Battisti, D. (2001). Disinfection, sterilization, and preservation. In S. Block (Ed.), Disinfection, sterilization, and preservation (5th ed., pp. 215-227). Philadelphia, PA: Lippincott Williams & Wilkins.