L’importance de la désinfection des sondes d’échographie endovaginales
Désinfection de haut niveau des sondes d’échographie endovaginales
Que sont les sondes endovaginales ?Les sondes endovaginales sont des dispositifs échographiques pelviens, qui utilisent des ondes à haute fréquence pour créer des images1. Elles permettent d’examiner les organes reproducteurs féminins, comme le vagin, le col de l’utérus, l’utérus, les trompes de Fallope et les ovaires, afin d’identifier des anomalies et de diagnostiquer des maladies1. Les examens réalisés avec une sonde endovaginale sont des examens internes qui impliquent d’introduire une sonde dans le vagin à une profondeur de 5 à 7,5 cm1 |
|
Pourquoi les sondes endovaginales nécessitent une désinfection de haut niveau ?
1. Recommandations de contrôle des infections
Les recommandations de contrôle des infections suivent la classification de Spaulding. Elle repose sur le risque infectieux des dispositifs utilisés dans les procédures sur des patients2. Lors de l’insertion d’une sonde endovaginale dans le vagin d’une patiente, la sonde touche les muqueuses intactes du col de l’utérus et de la paroi vaginale. Ainsi, selon la classification de Spaulding (Tableau 1.), les sondes endovaginales nécessitent une désinfection de haut niveau après utilisation2.
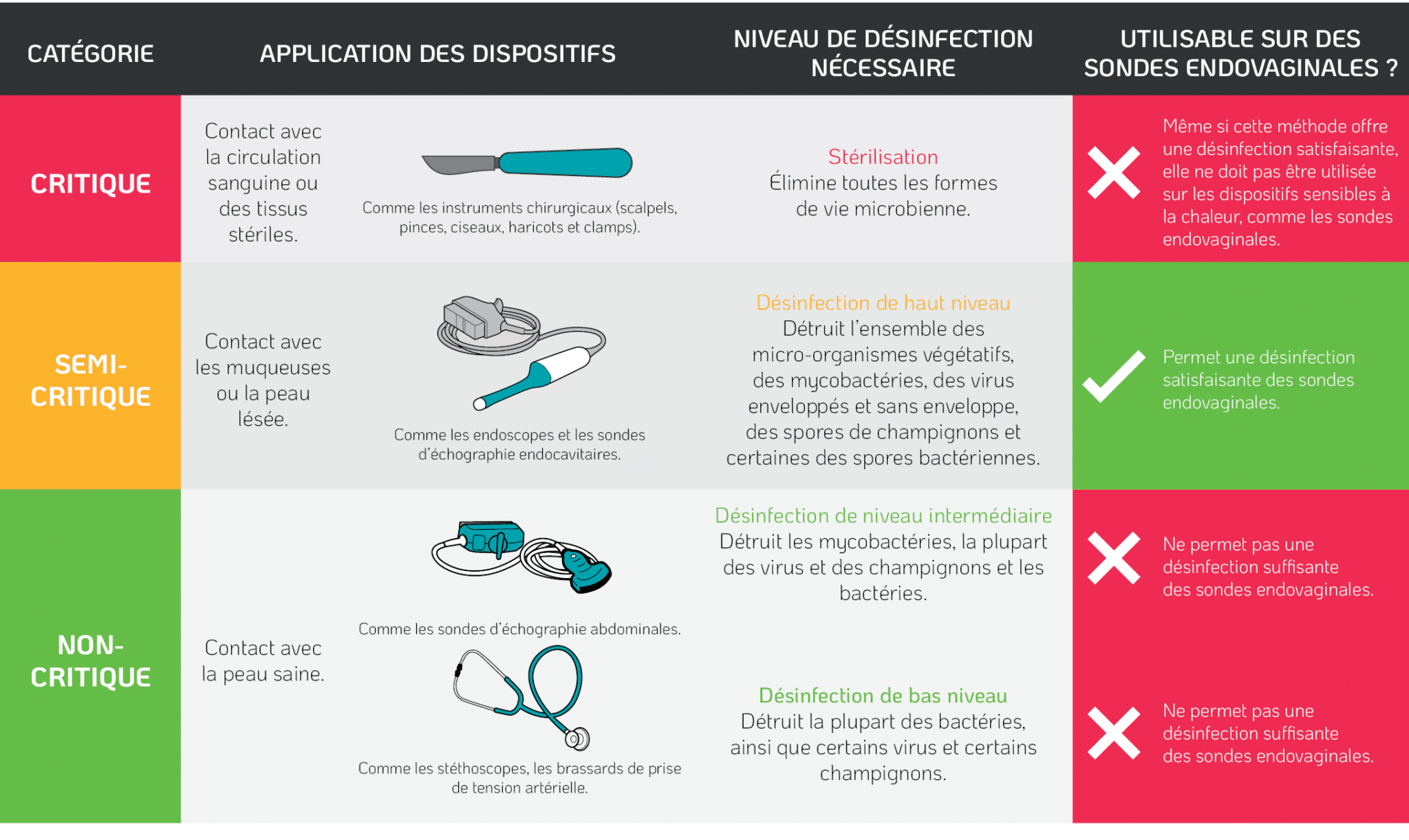
Table 1. La classification de Spaulding²
2. Risques de microperforation et de fuite du protège sonde
Les recommandations en vigueur dans le monde entier préconisent l’utilisation d’un protège-sonde afin de réduire les contaminations lors des procédures endovaginales3-12. La contamination reste cependant possible en raison des microperforations, d’une rupture partielle ou complète du protège-sonde pendant son utilisation ou d’un mauvais placement du protège-sonde sur la sonde (Figure 1.). Certains protège-sondes du commerce utilisés en échographie possèdent des taux de fuite inacceptablement élevés (jusqu’à 81 %) et n’offrent nullement une protection fiable contre les agents infectieux, en particulier les virus13.
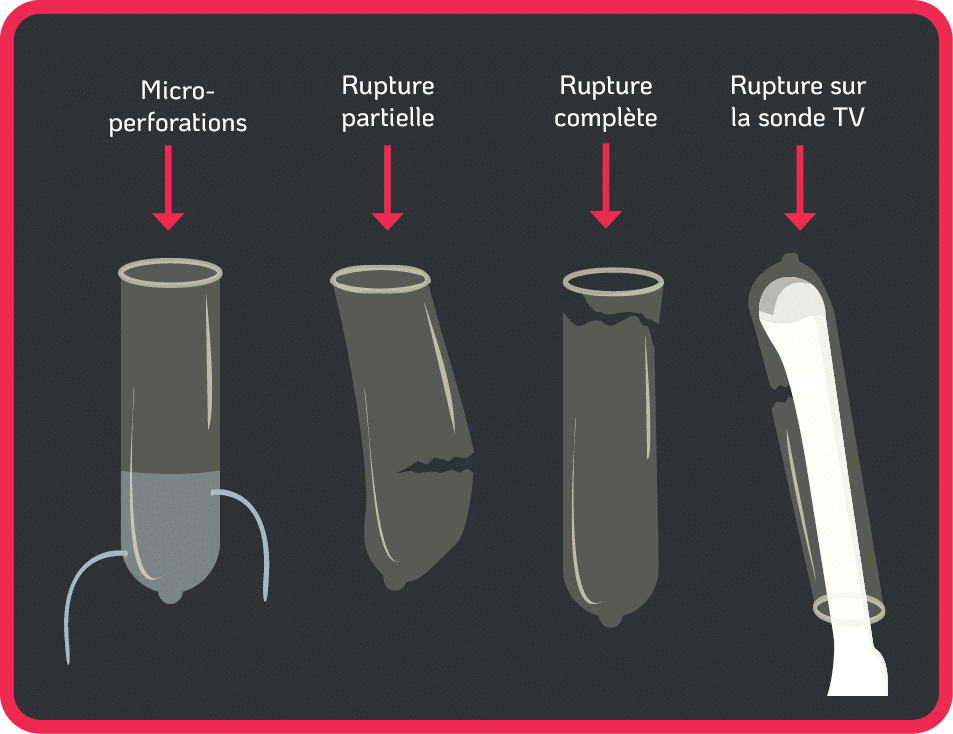
Figure 1. Risques de microperforation et de rupture du protège-sonde
La contamination peut subsister même lorsque la sonde endovaginale est protégée et fait l’objet d’une désinfection de niveau intermédiaire ou de bas niveau14-17. Si une sonde endovaginale n’est pas désinfectée de façon appropriée, si le protège-sonde comporte des microperforations ou des ruptures ou s’il n’est pas placé de manière appropriée, une transmission nosocomiale de patiente à patiente ou de patiente au professionnel de la santé risque de survenir. L’utilisation de désinfectants inappropriés sur les sondes ne réduit pas le niveau de contamination microbienne à un niveau sûr pour une utilisation sur la patiente suivante. Des agents pathogènes peuvent également être présents pendant une période prolongée en cas de désinfection insatisfaisante d’une surface ou d’un dispositif5. Par exemple, le papillomavirus humain (HPV) peut survivre jusqu’à sept jours sur les surfaces18.
3. Contamination du fil et de la prise de la sonde endovaginale
|
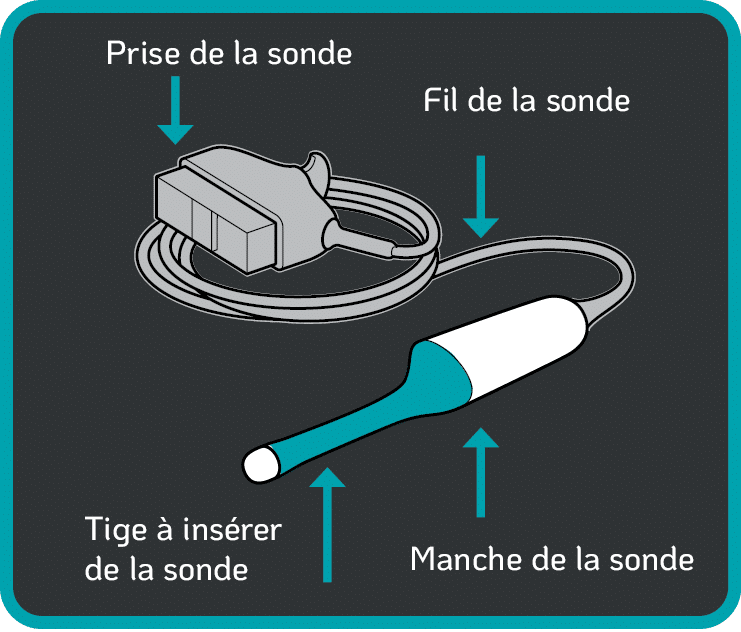
Voici les éléments d’une sonde endovaginale (Figure 2.) qui sont à risque de contamination sanguine ou microbienne : |
Figure 2. Éléments d’une sonde endovaginale standard |
4. Risques de spores bactériennes dans l’environnement
Les spores bactériennes, comme Bacillus subtilis, sont présentes dans notre environnement et sont considérées comme un contaminant environnemental22. Il n’est nécessaire de conserver ou de décontaminer les sondes endovaginales dans un endroit stérile, ce qui pourrait recontaminer les dispositifs après désinfection. Les spores bactériennes sont considérées comme les micro-organismes les plus résistants aux désinfectants (Figure 3) et la stérilisation est nécessaire pour détruire des taux élevés de spores. Etant donné que les sondes endovaginales ne tolèrent pas les températures élevées utilisées lors de la stérilisation et qu’elles peuvent être endommagées par la chaleur ainsi que par les produits chimiques agressifs, il est essentiel d’avoir recours à une solution appropriée telle que la désinfection de haut niveau.

Figure 3. Résistance des micro-organismes aux désinfectants. Adapté de Centers for Disease Control and Prevention (2008)2
La désinfection de haut niveau des sondes endovaginales réduit le risque de transmission de patiente à patiente et de patiente à professionnel de la santé
Une étude de Meyers et al. (2014) a démontré que les désinfectants de haut niveau mentionnés dans les recommandations mondiales de décontamination ne sont pas efficaces pour détruire le HPV23. Jusqu’à peu, il n’était pas possible de tester l’efficacité des désinfectants contre le HPV natif. En l’absence de méthodes disponibles, les organismes de réglementation recommandent d’effectuer des tests sur un polyomavirus SV40 de substitution, utilisé comme indicateur d’efficacité contre le HPV. Cependant, le profil de résistance aux désinfectants comparé des deux virus n’a pas été étudié. Cela signifie que l’efficacité contre le polyomavirus SV40 de substitution n’équivaut pas forcément à l’efficacité contre le HPV23.
La Société de Médecine Maternelle et Fœtale (Society for Maternal-Fetal Medicine) a récemment publié (2020) des recommandations concernant la sécurité des patientes. Ces recommandations portent sur la réduction du risque de transmission d’infections lors des examens réalisés avec une sonde endovaginale et préconisent de respecter les pratiques suivantes:
• Un usage unique des protège-sondes pour chaque examen avec sonde endovaginale13.
• Une utilisation de poches de gel d’échographie à usage unique stériles13.
• Le nettoyage, c’est-à-dire l’élimination des éléments contaminant comme le gel et les débris qui peuvent réduire l’efficacité
de la désinfection sur les sondes endovaginales après chaque examen13.
• La désinfection de haut niveau à l’aide d’un agent dont l’efficacité contre le HPV a été prouvée13.
Une étude scientifique de Meyers et al. (2020) démontre que Tristel Trio Wipes System et Tristel Duo ULT possèdent une efficacité contre l’infection à HPV16 et à HPV18 sur du matériel comme les sondes d’échographie endovaginales
en 30 secondes24.

 |
Tristel Trio Wipes SystemProduit de référence pour la décontamination manuelle des dispositifs médicaux invasifs sans canal opérteur et non invasifs. Temps de contact de 30 secondes Cliquez ici pour en savoir plus sur Tristel Trio Wipes System. |
|
|
|
… |
Tristel Duo ULTMousse désinfectante de haut niveau à base de ClO2 pour les sondes d’échographie endocavitaires et les transducteurs cutanés, dont les fils, les prises et les panneaux de commande. Temps de contact de 30 secondes Cliquez ici pour en savoir plus sur Tristel Duo ULT. |
References
1. NHS. 2018. Ultrasound Scan. [online] Available at: <https://www.nhs.uk/conditions/ultrasound-scan/> [Accessed 3 October 2020].
2. Centers for Disease Control and Prevention (2008) Guideline for Disinfection and Sterilization in Healthcare Facilities, 2008 Available at: https://www.cdc.gov/infectioncontrol/pdf/guidelines/disinfection-guidelines-H.pdf [Accessed 3 October 2020]
3. Abramowicz JS, Evans DH, Fowlkes JB, Marsal K, TerHaar G, on behalf of the WFUMB Safety Committee. Guidelines for cleaning transvaginal ultrasound transducers between patients. Ultrasound in Med & Biol, 2017; 43(5):1076-1079.
4. EFSUMB (European Federation of Societies for Ultrasound in Medicine and Biology) -2017; http://www.efsumb.org/safety/resources/2017-probe_cleaning.pdf.
5. Prevention Du Risque Infectieux Associe Aux Actes D’echographie Endocavitaire https://solidarites-sante.gouv.fr/IMG/pdf/fiches_sondes.pdf.
6. Nyhsen, C., Humphreys, H., Koerner, R., Grenier, N., Brady, A., Sidhu, P., Nicolau, C., Mostbeck, G., D’Onofrio, M., Gangi, A. and Claudon, M., 2017. Infection prevention and control in ultrasound – best practice recommendations from the European Society of Radiology Ultrasound Working Group. Insights into Imaging, 8(6), pp.523-535.
7. Guidelines for reprocessing ultrasound transducers AJUM, 2017, 20;1:30-40.
8. BMUS / SOR (British Medical Ultrasound Society / Society and College of Radiology) -2017; https://www.bmus.org/policies-statements-guidelines/professional-guidance/guidelines-for-professional-ultrasound-practice/
9. Irish Health Service Executive (HSE) Quality Improvement Division – Decontamination Safety Programme (2017) HSE guidance for decontamination of semi‐critical ultrasound probes; Semi‐invasive and Non‐invasive Ultrasound Probes QPSD-GL-028-1 http://wwwhseie/eng/about/Who/QID/nationalsafetyprogrammes/decontamination/Ultrasound-Probe-Decontamination-Guidance-Feb-17pdf
10. Health Facilities Scotland Decontamination Services (2016) NHS Scotland guidance for decontamination of semi-critical ultrasound probes; semi-invasive and non-invasive ultrasound probes http://wwwhpsscotnhsuk/documents/hai/infectioncontrol/guidelines/NHSScotland-Guidance-for-Decontaminationof-Semi-Critical-Ultrasound-Probespdf
11. Guidelines for Reprocessing Ultrasound Transducers by the Australasian Society for Ultrasound in Medicine and the Australasian College for Infection Prevention and Control (2017) AJUM 20 (1) http://onlinelibrary.wiley.com/doi/10.1002/ajum.12042/epdf
12. Rutala WA, Weber D. Reprocessing semicritical items. Am J Infect Control. 2016;44:e53–e62. doi: 10.1016/j.ajic.2015.12.029.
13. Hamm, R., Combs, C. and Davidson, C., 2020. Society for Maternal-Fetal Medicine Special Statement: Reducing the risk of transmitting infection by transvaginal ultrasound examination. American Journal of Obstetrics and Gynecology, 223(3), pp.B2-B6.
14. M’Zali, F., Bounizra, C., Leroy, S., Mekki, Y., Quentin-Noury, C., Kann, M. (2014) ‘Persistence of MicrobialContamination on Transvaginal Ultrasound Probes despite Low-Level Disinfection Procedure’, PLoS ONE, vol. 9, no. 4 [Online]. DOI: 10.1371/journal.pone.0093368 (Accessed 17 June 2018).
15. Ma, S., Yeung, A., Chan, P., Graham, C. (2014) High level disinfection reduces HPV contamination of transvaginal sonography probes in the emergency department [Online]. Available at: https://emj.bmj.com/content/30/6/472.responses#high-level-disinfection-reduces-hpv-contamination-of-transvaginal-sonography-probes-in-the-emergency-department (Accessed 26 July 2018).
16. Casalegno, JS., Carval, K., Eibach, D., Valdeyron, ML., Lamblin, G., Jacquemoud, H., Mellier, G., Lina, B., Gaucherand, P., Mathevet, P., Mekki1, Y. (2012) ‘High Risk HPV Contamination of Endocavity Vaginal Ultrasound Probes: An Underestimated Route of Nosocomial Infection?’, PLoS ONE, vol. 7, no. 10 [Online]. DOI: doi:10.1371/journal.pone.0048137 (Accessed 23 June 2018).
17. Strauss, S., Sastry, P., Sonnex, C., Edwards, S, Gray, J. (2002) ‘Contamination of environmental surfaces by genital human papillomaviruses’,
18. Roden, R., Lowy, D., Schiller, J. (1997) ‘Papillomavirus Is Resistant to Desiccation’, The Journal of Infectious Diseases, vol. 176, no. 5., pp. 1076-1079 [Online] DOI: https://doi.org/10.1086/516515
19. Basseal, J., Westerway, S. and Hyett, J., 2020. Analysis of the integrity of ultrasound probe covers used for transvaginal examinations. Infection, Disease & Health, 25(2), pp.77-81
20. Westerway, S. C., Basseal, J. M., Brockway, A., Hyett, J. A., Carter, D. A. (2016) ‘Potential Infection Control Risks Associated with Ultrasound Equipment – A Bacterial Perspective’, Ultrasound in Medicine & Biology [Online] DOI: 10.1016/j.ultrasmedbio.2016.09.004 (Accessed 25 October 2018).
21. Keys, M., Sim, B., Thom, O., Tunbridge, M., Barnett, A., Fraser, J. (2015) ‘Efforts to Attenuate the Spread of Infection (EASI): a prospective, observational multicentre survey of ultrasound equipment in Australian emergency departments and intensive care units’, Critical care and resuscitation, vol. 17, no. 1, pp. 43-46 [Online]. Available at: https://www.ncbi.nlm.nih.gov/pubmed/25702761 (Accessed 04 April 2019).
22. Allos, B.M., Blaser, M.J., Platts-Mills, J. and Kosek, M., 2014. Campylobacter Species – Infectious Disease and Antimicrobial Agents. [online] Antimicrobe.org. Available at: http://www.antimicrobe.org/new/b91.asp [Accessed 5 August 2020].
23. Meyers, J., Ryndock, E., Conway, M., Meyers, C. and Robison, R., 2014. Susceptibility of high-risk human papillomavirus type 16 to clinical disinfectants. Journal of Antimicrobial Chemotherapy, 69(6), pp.1546-1550.
24. Meyers, C., Milici, J., Robison, R. (2020) ‘The Ability of Two Chlorine Dioxide Chemistries to Inactivate Human Papillomavirus-contaminated Endocavitary Ultrasound Probes and Nasendoscopes’. Published IN THE JOURNAL OF MEDICAL VIROLOGY [Online] Available at: bit.ly/HPVARTICLE
25. World Health Organization. 2018. Human Papillomavirus (HPV). [online] Available at: <https://www.who.int/immunization/diseases/hpv/en/> [Accessed 19 October 2020].
©2021 Tristel Solution Limited. All rights reserved.