Het belang van high-level desinfectie van transvaginale echoprobes
HET BELANG VAN HIGH-LEVEL DESINFECTIE (HLD) VAN TRANSVAGINALE (TV) ECHOPROBES
Wat zijn TV echoprobes?TV Echoprobes zijn apparaten voor bekkenbodem echografie die gebruikmaken van hoogfrequente geluidsgolven om beelden te maken1. Ze maken het onderzoek van de vrouwelijke geslachtsorganen mogelijk, zoals de vagina, baarmoederhals, baarmoeder, eileiders en eierstokken, om afwijkingen te kunnen identificeren en aandoeningen te diagnosticeren. Tijdens een transvaginaal onderzoek, dat inwendig is, wordt de sonde ongeveer vijf tot tien centimeter in de vagina ingebracht1. |
|
Waarom is HLD noodzakelijk voor TV echoprobes?
1. Bekrachtiging van de richtlijnen voor infectiepreventie
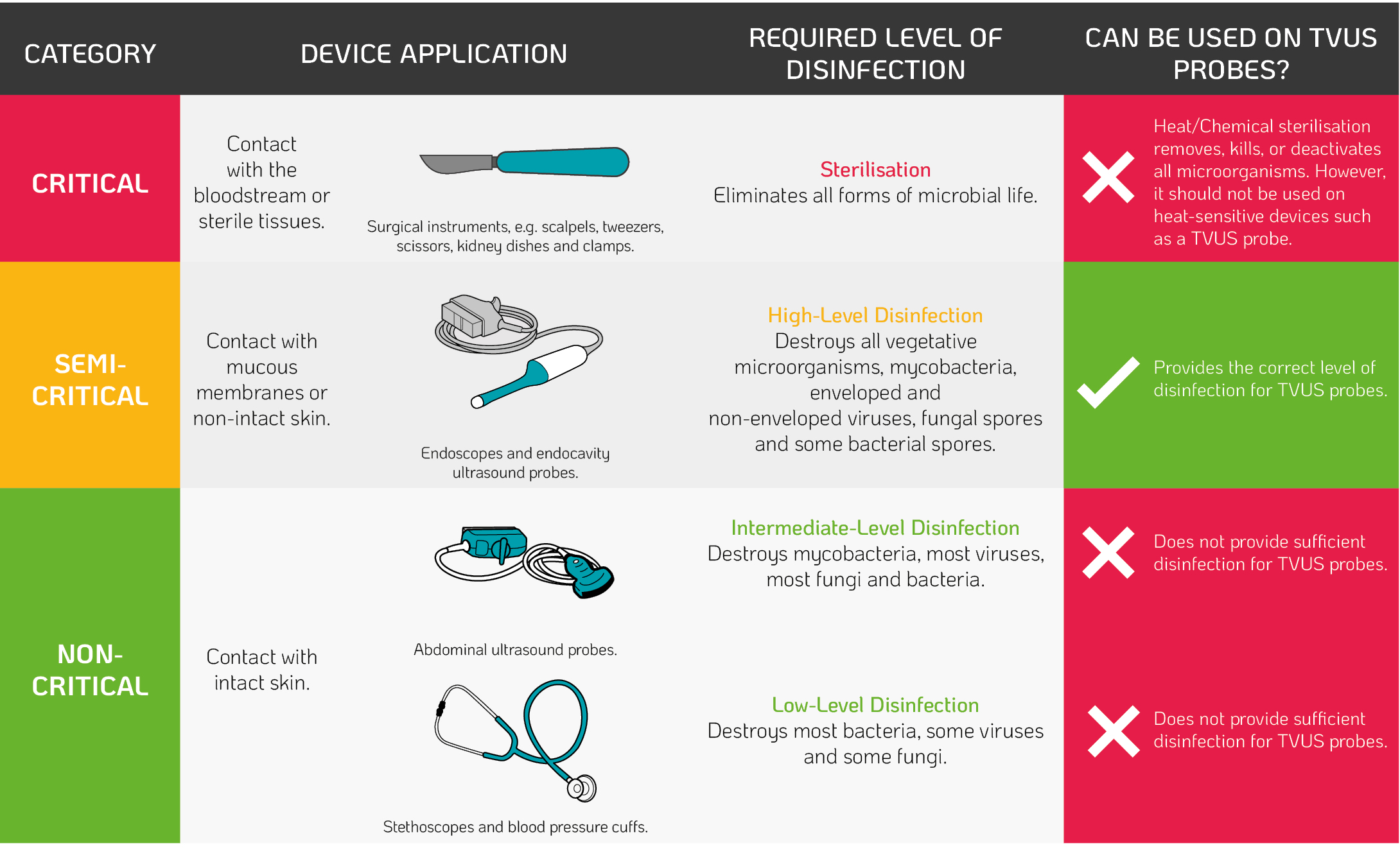
Bij het aanbevelen van desinfectie- of sterilisatiemethoden volgen de richtlijnen voor infectiepreventie de Spaulding-classificatie. Deze classificatie is gebaseerd op het infectierisico van apparaten die worden gebruikt bij een procedure met een patiënt2. Bij het inbrengen in de patiënt komen tv echoprobes in contact met het intacte slijmvlies van de baarmoederhals en de vaginawand. Volgens de Spaulding-classificatie (tabel 1) is high-level desinfectie van echoprobes daarom noodzakelijk na gebruik2.
Tabel 1. De Spaulding Classificatie²
2. Microperforatie en lekkagerisico’s bij beschermhoezen
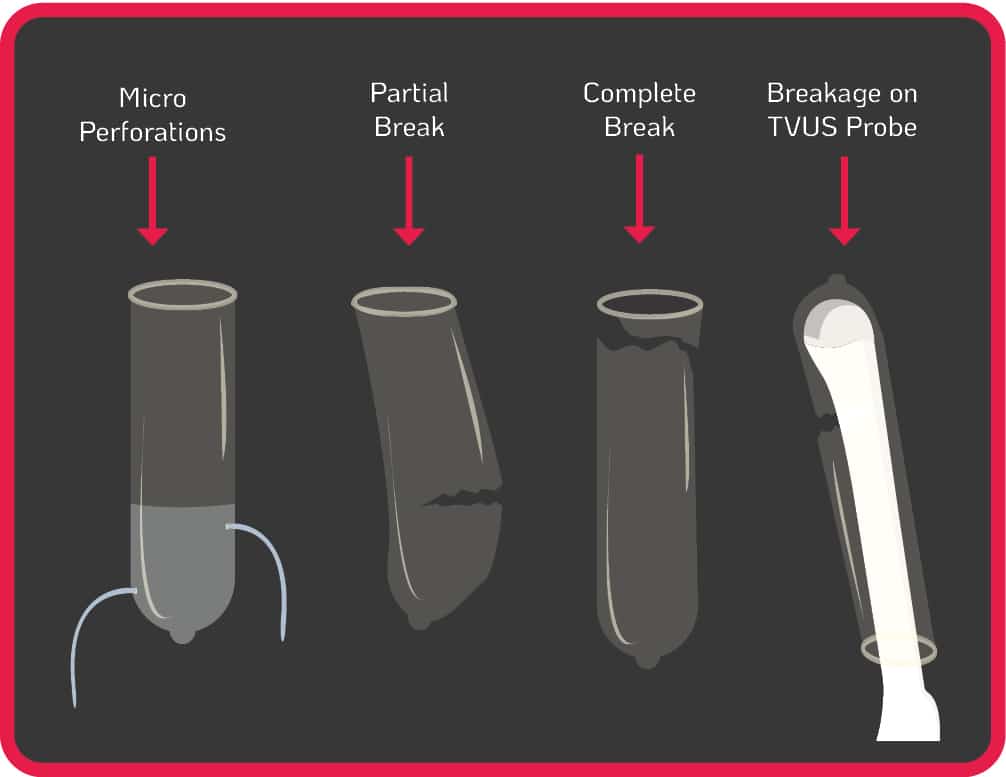
Het gebruik van beschermhoezen wordt wereldwijd bekrachtigd door richtlijnen om besmetting te minimaliseren tijdens de uitvoering van echografieën3-12. Contaminatie kan nog steeds optreden als gevolg van microperforaties, gedeeltelijk of volledig scheuren van de hoes tijdens gebruik of onjuiste plaatsing van de hoes op de probe (zie afbeelding 1). Sommige commercieel geproduceerde hoezen voor echoprobes hebben een onaanvaardbaar hoog lekkage percentage (tot 81 %) en vormen geen betrouwbare barrière tegen infectieuze micro-organismen, met name virussen13.
Figuur 1. Micro Perforation & Probe Cover Leakage Risks
Residuele contaminatie is mogelijk, zelfs wanneer de echoprobe wordt afgedekt en gedesinfecteerd met desinfectiemiddelen van gemiddeld of laag niveau14-17. Als een echoprobe niet voldoende wordt gedesinfecteerd tussen elk patiëntonderzoek in, als hoezen microperforaties hebben of scheuren of als hoezen niet correct worden geplaatst, kan nosocomiale overdracht plaatsvinden van patiënt op patiënt, of van patiënt op zorgverlener. Het gebruik van ontoereikende desinfectiemiddelen op probes zal het niveau van microbiële besmetting niet doen dalen tot een niveau dat veilig is voor gebruik bij de volgende patiënt. Pathogenen kunnen langdurig aanwezig blijven als een oppervlak of apparaat niet naar behoren wordt gedesinfecteerd. Zo kan het humaan papillomavirus (HPV) tot zeven dagen overleven op oppervlakken18.
3. Contaminatie van de kabel en stekker van tv echoprobes
|
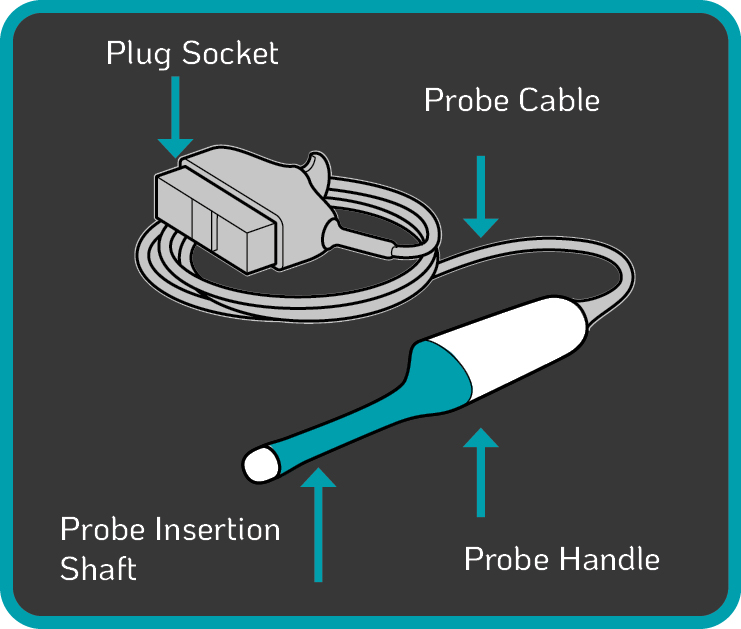
Onderdelen van de echoprobe (afbeelding 2.) die risico lopen op contaminatie met bloed en bacteriën zijn onder meer: • de inbrengschacht, die bij de patiënt wordt ingebracht20,21 • de handgreep van het apparaat20,21 • de kabel en de stekker20,21 • de houder van het apparaat High-level desinfectie voorkomt de verspreiding van schadelijke pathogenen van patiënt op patiënt, maar beschermt ook de zorgverleners tijdens de procedures. Sommige automatische desinfectieapparaten kunnen alleen de inbrengschacht van de echosonde desinfecteren. Het Tristel Duo ULT en Tristel Trio Wipes systeem zijn ontworpen om de hele probe vanaf de stekker en de kabel tot de inbrengschacht te desinfecteren. |
Figuur 2. Components of a Standard TVUS Probe |
4. Risico op bacteriële sporen uit de omgeving
Bacteriële sporen zoals Bacillus subtilis zijn overal rondom ons aanwezig en worden beschouwd als een omgevingscontaminant22. Echoprobes moeten niet worden bewaard of gedesinfecteerd in een steriele ruimte. Dit kan ervoor kan zorgen dat apparaten na desinfectie opnieuw worden gecontamineerd. Bacteriële sporen worden beschouwd als de meest resistente micro-organismen tegen desinfectantia (afbeelding 3) en sterilisatie is noodzakelijk om de hoge hoeveelheden sporen te doden. Echoprobes zijn niet bestand tegen de hoge temperaturen die bij sterilisatie worden gebruikt. Verhitting en bijtende chemische stoffen kunnen de probe beschadigen. Daarom moet een geschikte oplossing voor high-level desinfectie worden gebruikt.

Adapted from Centers for Disease Control and Prevention (2008)2
High-level Desinfectie van tv echoprobes vermindert het risico op infectieoverdracht
In een studie van Meyers et al., (2014) is aangetoond dat de high-level desinfectiemiddelen die in de wereldwijde richtlijnen voor desinfectie zijn opgenomen, niet werkzaam zijn tegen HPV23. Tot voor kort was het niet mogelijk om de werkzaamheid van desinfectiemiddelen tegen het échte HPV te testen. Bij gebrek aan beschikbare methoden raden regelgevende instanties aan om te testen tegen het surrogaat polyomavirus SV40, dat als een indicator voor de werkzaamheid tegen HPV wordt gebruikt. De resistentieprofielen van deze twee virussen tegen desinfectiemiddelen werden echter niet onderzocht. Dit betekent dat de werkzaamheid tegen het surrogaat polyomavirus SV40 niet noodzakelijk werkzaamheid tegen HPV impliceert23.
De Society for Maternal-Fetal Medicine (2020) heeft onlangs een richtlijn voor patiëntveiligheid gepubliceerd om het risico op overdracht van infecties via transvaginale echografieonderzoeken te reduceren en beveelt het volgende aan:
• Eenmalig gebruik van steriele probehoezen voor elk transvaginaal onderzoek13.
• Gebruik van steriele ultrasone gelpakketten voor eenmalig gebruik13.
• Reiniging, d.w.z. het verwijderen van grove verontreiniging, zoals gel en vuil, dat de werkzaamheid van een desinfectans kan verminderen op echoprobes na elk onderzoek13.
• High-level desinfectie met een middel met bewezen werkzaamheid tegen HPV13.
Een wetenschappelijke studie van Meyers, et al. (2020) toont aan dat het Tristel Trio Wipes Systeem en Tristel Duo ULT binnen 30 seconden werkzaam zijn tegen HPV-types 16 en 18 op een transvaginale echoprobe24.
 |
Tristel Trio Wipes SystemDe gouden standaard voor de manuele desinfectie van invasieve en niet-invasive medische hulpmiddelen zonder werkkanaal. contacttijd van 30 seconden Klik hier voor meer info over het Tristel Trio Wipes System |
|
|
|
… |
Tristel Duo ULTEen high-level desinfectie-schuim op basis van chloordioxide voor transvaginale en transrectaleechoprobes, inclusief stekker, kabel en houder. contacttijd van 30 seconden Klik hier voor meer informatie over Tristel Duo ULT |
Referenties
1. NHS. 2018. Ultrasound Scan. [online] Available at: <https://www.nhs.uk/conditions/ultrasound-scan/> [Accessed 3 October 2020].
2. Centers for Disease Control and Prevention (2008) Guideline for Disinfection and Sterilization in Healthcare Facilities, 2008 Available at: https://www.cdc.gov/infectioncontrol/pdf/guidelines/disinfection-guidelines-H.pdf [Accessed 3 October 2020]
3. Abramowicz JS, Evans DH, Fowlkes JB, Marsal K, TerHaar G, on behalf of the WFUMB Safety Committee. Guidelines for cleaning transvaginal ultrasound transducers between patients. Ultrasound in Med & Biol, 2017; 43(5):1076-1079.
4. EFSUMB (European Federation of Societies for Ultrasound in Medicine and Biology) -2017; http://www.efsumb.org/safety/resources/2017-probe_cleaning.pdf.
5. Prevention Du Risque Infectieux Associe Aux Actes D’echographie Endocavitaire https://solidarites-sante.gouv.fr/IMG/pdf/fiches_sondes.pdf.
6. Nyhsen, C., Humphreys, H., Koerner, R., Grenier, N., Brady, A., Sidhu, P., Nicolau, C., Mostbeck, G., D’Onofrio, M., Gangi, A. and Claudon, M., 2017. Infection prevention and control in ultrasound – best practice recommendations from the European Society of Radiology Ultrasound Working Group. Insights into Imaging, 8(6), pp.523-535.
7. Guidelines for reprocessing ultrasound transducers AJUM, 2017, 20;1:30-40.
8. BMUS / SOR (British Medical Ultrasound Society / Society and College of Radiology) -2017; https://www.bmus.org/policies-statements-guidelines/professional-guidance/guidelines-for-professional-ultrasound-practice/
9. Irish Health Service Executive (HSE) Quality Improvement Division – Decontamination Safety Programme (2017) HSE guidance for decontamination of semi‐critical ultrasound probes; Semi‐invasive and Non‐invasive Ultrasound Probes QPSD-GL-028-1 http://wwwhseie/eng/about/Who/QID/nationalsafetyprogrammes/decontamination/Ultrasound-Probe-Decontamination-Guidance-Feb-17pdf
10. Health Facilities Scotland Decontamination Services (2016) NHS Scotland guidance for decontamination of semi-critical ultrasound probes; semi-invasive and non-invasive ultrasound probes http://wwwhpsscotnhsuk/documents/hai/infectioncontrol/guidelines/NHSScotland-Guidance-for-Decontaminationof-Semi-Critical-Ultrasound-Probespdf
11. Guidelines for Reprocessing Ultrasound Transducers by the Australasian Society for Ultrasound in Medicine and the Australasian College for Infection Prevention and Control (2017) AJUM 20 (1) http://onlinelibrary.wiley.com/doi/10.1002/ajum.12042/epdf
12. Rutala WA, Weber D. Reprocessing semicritical items. Am J Infect Control. 2016;44:e53–e62. doi: 10.1016/j.ajic.2015.12.029.
13. Hamm, R., Combs, C. and Davidson, C., 2020. Society for Maternal-Fetal Medicine Special Statement: Reducing the risk of transmitting infection by transvaginal ultrasound examination. American Journal of Obstetrics and Gynecology, 223(3), pp.B2-B6.
14. M’Zali, F., Bounizra, C., Leroy, S., Mekki, Y., Quentin-Noury, C., Kann, M. (2014) ‘Persistence of MicrobialContamination on Transvaginal Ultrasound Probes despite Low-Level Disinfection Procedure’, PLoS ONE, vol. 9, no. 4 [Online]. DOI: 10.1371/journal.pone.0093368 (Accessed 17 June 2018).
15. Ma, S., Yeung, A., Chan, P., Graham, C. (2014) High level disinfection reduces HPV contamination of transvaginal sonography probes in the emergency department [Online]. Available at: https://emj.bmj.com/content/30/6/472.responses#high-level-disinfection-reduces-hpv-contamination-of-transvaginal-sonography-probes-in-the-emergency-department (Accessed 26 July 2018).
16. Casalegno, JS., Carval, K., Eibach, D., Valdeyron, ML., Lamblin, G., Jacquemoud, H., Mellier, G., Lina, B., Gaucherand, P., Mathevet, P., Mekki1, Y. (2012) ‘High Risk HPV Contamination of Endocavity Vaginal Ultrasound Probes: An Underestimated Route of Nosocomial Infection?’, PLoS ONE, vol. 7, no. 10 [Online]. DOI: doi:10.1371/journal.pone.0048137 (Accessed 23 June 2018).
17. Strauss, S., Sastry, P., Sonnex, C., Edwards, S, Gray, J. (2002) ‘Contamination of environmental surfaces by genital human papillomaviruses’,
18. Roden, R., Lowy, D., Schiller, J. (1997) ‘Papillomavirus Is Resistant to Desiccation’, The Journal of Infectious Diseases, vol. 176, no. 5., pp. 1076-1079 [Online] DOI: https://doi.org/10.1086/516515
19. Basseal, J., Westerway, S. and Hyett, J., 2020. Analysis of the integrity of ultrasound probe covers used for transvaginal examinations. Infection, Disease & Health, 25(2), pp.77-81
20. Westerway, S. C., Basseal, J. M., Brockway, A., Hyett, J. A., Carter, D. A. (2016) ‘Potential Infection Control Risks Associated with Ultrasound Equipment – A Bacterial Perspective’, Ultrasound in Medicine & Biology [Online] DOI: 10.1016/j.ultrasmedbio.2016.09.004 (Accessed 25 October 2018).
21. Keys, M., Sim, B., Thom, O., Tunbridge, M., Barnett, A., Fraser, J. (2015) ‘Efforts to Attenuate the Spread of Infection (EASI): a prospective, observational multicentre survey of ultrasound equipment in Australian emergency departments and intensive care units’, Critical care and resuscitation, vol. 17, no. 1, pp. 43-46 [Online]. Available at: https://www.ncbi.nlm.nih.gov/pubmed/25702761 (Accessed 04 April 2019).
22. Allos, B.M., Blaser, M.J., Platts-Mills, J. and Kosek, M., 2014. Campylobacter Species – Infectious Disease and Antimicrobial Agents. [online] Antimicrobe.org. Available at: http://www.antimicrobe.org/new/b91.asp [Accessed 5 August 2020].
23. Meyers, J., Ryndock, E., Conway, M., Meyers, C. and Robison, R., 2014. Susceptibility of high-risk human papillomavirus type 16 to clinical disinfectants. Journal of Antimicrobial Chemotherapy, 69(6), pp.1546-1550.
24. Meyers, C., Milici, J., Robison, R. (2020) ‘The Ability of Two Chlorine Dioxide Chemistries to Inactivate Human Papillomavirus-contaminated Endocavitary Ultrasound Probes and Nasendoscopes’. Published IN THE JOURNAL OF MEDICAL VIROLOGY [Online] Available at: bit.ly/HPVARTICLE
25. World Health Organization. 2018. Human Papillomavirus (HPV). [online] Available at: <https://www.who.int/immunization/diseases/hpv/en/> [Accessed 19 October 2020].
©2021 Tristel Solution Limited. All rights reserved.