La lutte contre la résistance aux antimicrobiens : désinfectons responsablement
La lutte contre la résistance aux antimicrobiens (RAM) est cruciale pour la santé mondiale. Cet article met en avant l’importance d’adopter des pratiques de désinfection efficaces pour empêcher la propagation des bactéries résistantes. Découvrez comment des solutions innovantes, telles que les désinfectants sporicides et de haut niveau Tristel, offrent une protection fiable contre la RAM, pour désinfecter responsablement.

La résistance aux antimicrobiens (RAM) représente un défi crucial pour la santé publique mondiale. En 2019, elle a été la cause directe de plus de 1,27 million de décès et a contribué à 4,95 millions d’autres. Outre son impact sur la santé humaine, la RAM a également des répercussions économiques significatives. Sans intervention, les coûts liés aux soins de santé et aux pertes de productivité pourraient atteindre 1 000 milliards de dollars d’ici 2050.1
Notre société se trouve face à une urgence… De nouvelles prévisions suggèrent que la RAM causera 39 millions de décès entre 2025 et 2050, ce qui équivaut à 3 décès par minute.2
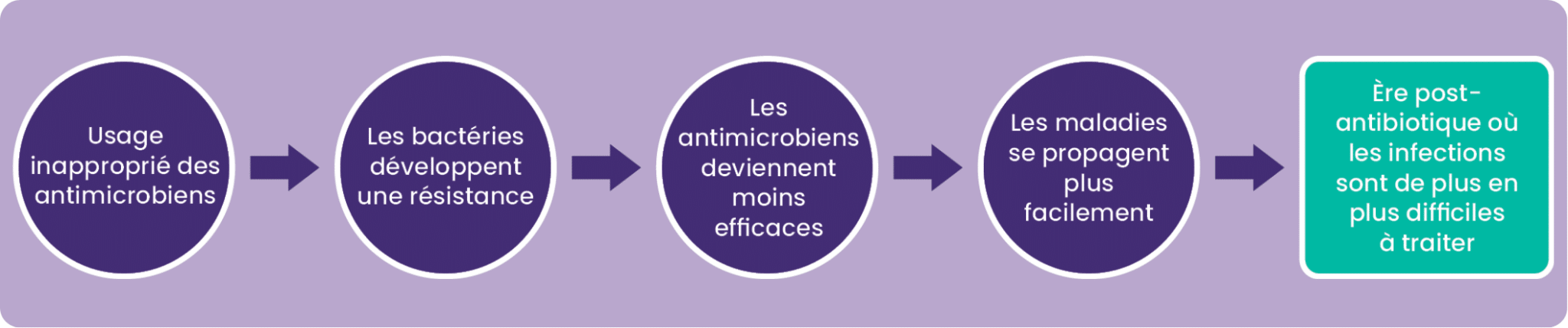
Sans actions concrètes, nous risquons d’entrer dans une ère « post-antibiotique » où les infections courantes deviendront impossibles à traiter.
Les antibiotiques sont une des causes de la RAM
La RAM trouve notamment son origine dans la prescription excessive et l’utilisation inappropriée des antibiotiques. Plus ces médicaments sont employés fréquemment et de manière abusive, plus le risque de développement de bactéries résistantes est élevé. C’est sans compter qu’une utilisation incorrecte des antibiotiques, comme l’interruption prématurée d’un traitement, permet aux bactéries de survivre et de développer une résistance.
Au-delà des antibiotiques, les biocides sont également remis en question
Les antibiotiques ne sont pas les seuls mis en cause. L’utilisation de certains biocides pour la désinfection des dispositifs médicaux et des surfaces, notamment le recours aux Composés d’Ammonium Quaternaire (CAQs) est également pointée du doigt.3
Les CAQs sont des agents tensioactifs chargés positivement efficaces contre un spectre limité de micro-organismes (principalement les bactéries, les levures et les virus enveloppés) qui agissent en se liant à leur membrane cellulaire. Après un certain temps, cette paroi peut être pénétrée, ce qui entraîne une rupture de la membrane et une fuite de son contenu.
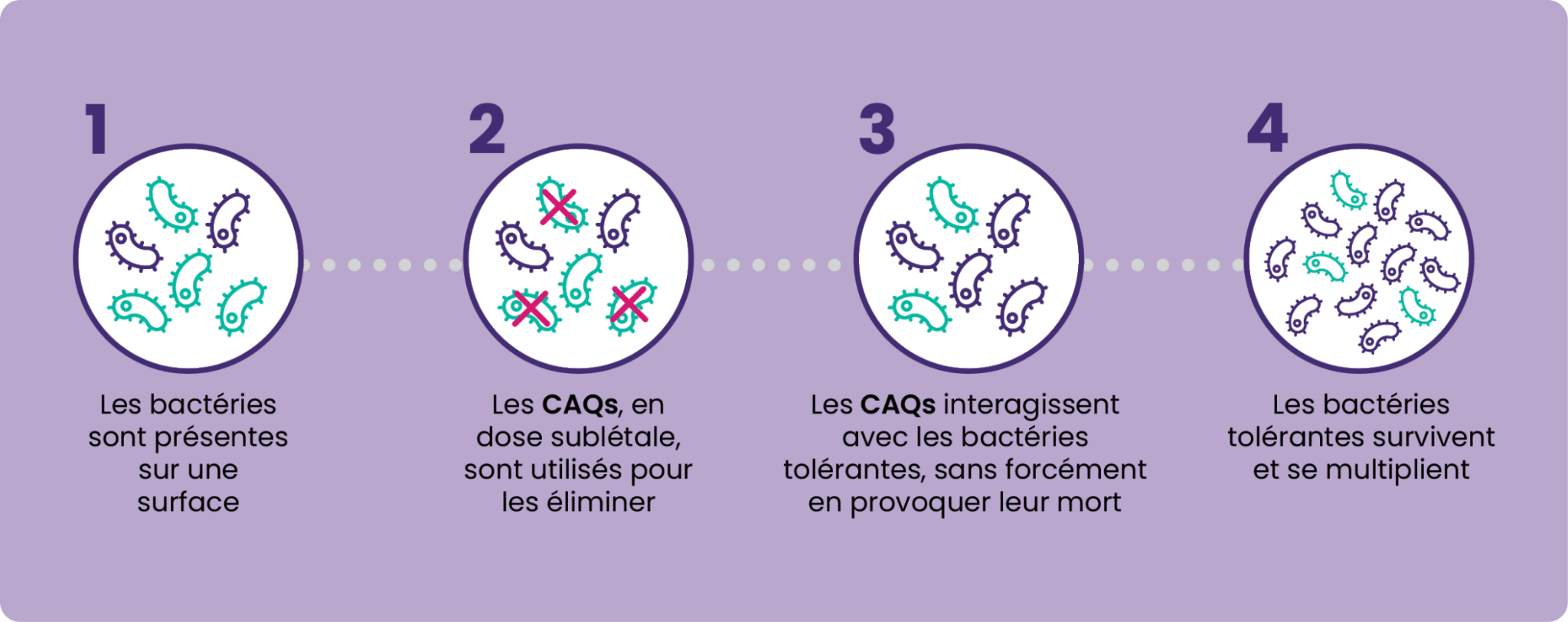
En termes simples, les CAQs se frayent un chemin à l’intérieur des micro-organismes pour en provoquer leur mort. Cette perturbation ne se produit pas immédiatement ou à chaque concentration. Dans de nombreux cas, elle ne se produit que lorsque des concentrations élevées de CAQs ou des combinaisons de CAQs sont utilisées.
Dans tous les autres cas, les CAQs peuvent interagir avec les micro-organismes tolérants, mais pas au point d’en provoquer leur mort.
C’est dans cette zone grise que la RAM devient une menace réelle qui doit être surveillée de près.
Lorsqu’un micro-organisme est exposé à de faibles concentrations d’un biocide sans être éliminé, il peut y développer une immunité, un phénomène connu sous le nom de résistance bactérienne acquise.
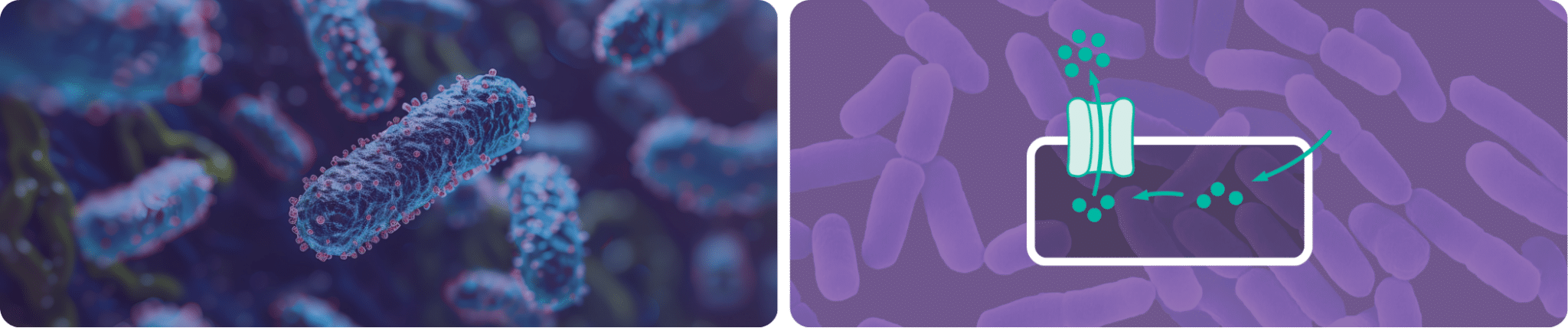
Génétiquement, le micro-organisme peut manifester des structures appelées pompes d’efflux, permettant aux cellules de réguler leur environnement interne en éliminant activement les agents désinfectants qui y entreraient. Cela diminue leur effet toxique et favorise la survie des micro-organismes dans un environnement contenant des doses sublétales de désinfectants.
Cette résistance bactérienne acquise ne se limite pas à un seul micro-organisme. Celui qui a appris à se défendre transmettra son gène de résistance à sa descendance ou à ses congénères par simple contact avec d’autres micro-organismes d’une même espèce ou d’une espèce différente.4
Quel lien existe-t-il entre la tolérance aux désinfectants et la résistance aux antibiotiques?
Un micro-organisme qui a acquis une résistance à un agent désinfectant particulier peut également utiliser des mécanismes similaires pour résister à d’autres antimicrobiens, dont les antibiotiques font partie.5 On fait ici référence à la co-résistance ou résistance croisée.
Ainsi, si un micro-organisme qui était éliminé par un simple spray ou une lingette désinfectante ne peut plus être éliminé, le risque qu’il survive et qu’il infecte une personne devient considérablement plus élevé. Si ce même micro-organisme fait appel à son mécanisme de résistance acquise pour contrer l’effet d’un antibiotique, alors il risque de nous faire basculer dans cette ère où les infections courantes deviennent impossibles à traiter.
Les désinfectants qui nous protégeaient dans une certaine mesure autrefois pourraient bien mettre en péril notre système de santé en favorisant la RAM.
Que pouvons-nous mettre en place pour prévenir la résistance aux antibiotiques et la tolérance aux désinfectants ?
En premier lieu, il est important de limiter les doses subinhibitrices, c’est à dire insuffisamment puissantes pour obtenir l’effet désiré. Ce faible dosage détruira certains micro-organismes, mais ceux qui survivront seront moins sensibles aux antimicrobiens utilisés.6,7,8 Si ce processus devait se poursuivre, la concentration active d’antimicrobiens risquerait de devenir inefficace.
Dans le cas des biocides pour la désinfection des surfaces, les solutions aux dilutions variables sont particulièrement problématiques. Elles ne nous permettent pas d’être certain d’avoir choisi la concentration adaptée, c’est-à-dire suffisamment puissante et efficace contre tous les types de micro-organismes potentiellement présents sur une surface donnée.
En deuxième lieu, il convient d’éviter les désinfectants aux temps de contact variables et prolongés. Un long temps de contact avec un biocide doté d’une faible réactivité chimique expose les micro-organismes à des concentrations sublétales. Ceci favorise la survie de micro-organismes infectieux dont la susceptibilité aux antimicrobiens est diminuée.
Pour éviter les risques de résistance, il est donc préférable de se tourner vers des solutions au taux de dilution unique et dont l’efficacité est prouvée contre le spectre complet de micro-organismes en un temps de contact court et uniforme.
Les désinfectants de haut niveau et sporicides Tristel à base de dioxyde de chlore (ClO₂) se distinguent dans le monde de la chimie de par leur efficacité et leur mode d’action.
Le ClO₂ est en effet un biocide efficace contre les bactéries, les virus, les protozoaires, les levures, les fungi, les mycobactéries et les spores bactériennes.
Contrairement aux CAQs, la capacité du ClO₂ Tristel à tuer un spectre complet de micro-organismes est bien établie, sans nécessiter d’ajustement de concentration par les utilisateurs et sans temps de contact variables ou prolongés. L’efficacité contre les micro-organismes est quasi immédiate (entre 30 secondes et 5 minutes en fonction du produit) et se réalise à un taux de concentration unique (entre 100 et 200 ppm en fonction du produit).
L’utilisation d’un désinfectant de haut niveau et sporicide Tristel est-elle excessive pour traiter tous les risques infectieux, même ceux de bas niveau ?
L’utilisation quotidienne du ClO₂ Tristel ne contribue pas à la RAM. Outre son spectre complet d’efficacité en un temps de contact court et uniforme et à un taux de concentration unique, l’activité microbicide du ClO₂ Tristel se distingue par son mode d’action, l’oxydation.
Le ClO₂ Tristel est un oxydant qui tue les agents pathogènes par échange d’électrons, en les séquestrant des structures vitales du micro-organisme telles que les parois cellulaires, les membranes, les organites et le matériel génétique. C’est cet échange qui provoque un déséquilibre moléculaire conduisant à la mort certaine des micro-organismes.
Contrairement aux CAQs, qui ne parviennent à les éliminer que sous certaines conditions, le ClO₂ Tristel les détruit toujours, même en cas d’utilisation répétée.9,10
L’utilisation quotidienne du ClO₂ Tristel comme désinfectant de haut niveau et sporicide ne participe pas au développement de la RAM. Au contraire, elle pourrait bien être une solution de lutte majeure pour les établissements de soins.
3 Boyce, J. M. (2023). Quaternary ammonium disinfectants and antiseptics: Tolerance, resistance, and potential impact on antibiotic resistance. Antimicrobial Resistance & Infection Control, 12(32). https://doi.org/10.1186/s13756-023-01241-z
4 Vega, N. M., & Gore, J. (2014). Collective antibiotic resistance: Mechanisms and implications. Current Opinion in Microbiology, 21, 28-34. https://doi.org/10.1016/j.mib.2014.09.003
5 Ortega Morente, E., Fernández-Fuentes, M. A., Grande Burgos, M. J., Abriouel, H., Pérez Pulido, R., & Gálvez, A. (2013). Biocide tolerance in bacteria. International Journal of Food Microbiology, 162(1), 13-25. https://doi.org/10.1016/j.ijfoodmicro.2012.12.028
6 Walsh, S. E., Maillard, J. Y., Russell, A. D., Catrenich, C. E., Charbonneau, D. L., & Bartolo, R. G. (2003). Development of bacterial resistance to several biocides and effects on antibiotic susceptibility. Journal of Hospital Infection, 55(2), 98-107.
7 Voumard, M., Venturelli, L., Borgatta, M., et al. (2020). Adaptation of Pseudomonas aeruginosa to constant sub-inhibitory concentrations of quaternary ammonium compounds. Environmental Science: Water Research & Technology, 6(4), 1139-1152.
8 Soumet, C., Meheust, D., Pissavin, C., et al. (2016). Reduced susceptibilities to biocides and resistance to antibiotics in food-associated bacteria following exposure to quaternary ammonium compounds. Journal of Applied Microbiology, 121(5), 1275-1281.
9 Noszticzius, Z., Wittmann, M., Kály-Kullai, K., Beregvári, Z., Kiss, I., Rosivall, L. and Szegedi, J. (2013). Chlorine Dioxide Is a Size-Selective Antimicrobial Agent. PLoS ONE, 8(11), p.e79157. https://doi.org/10.1371/journal.pone.0079157
10 Block, S., Knapp, J., & Battisti, D. (2001). Disinfection, sterilization, and preservation. In S. Block (Ed.), Disinfection, sterilization, and preservation (5th ed., pp. 215-227). Philadelphia, PA: Lippincott Williams & Wilkins.