
Biofilms vormen een enorme uitdaging in de voortdurende strijd tegen zorggerelateerde infecties (Healthcare-Associated Infections – HAI’s), omdat ze pathogenen toleranter maken voor conventionele reinigings- en desinfectiemethoden. De chloordioxide-producten van Tristel zijn specifiek getest op hun werkzaamheid tegen zowel natte als droge biofilms.
De Rol van Biofilms in de Gezondheidszorg
Biofilms zijn gestructureerde microbiële gemeenschappen die zijn ingekapseld in een zelf aangemaakte matrix, en vaak aan oppervlakken in zorgomgevingen vastzitten. Eenmaal gevormd, zijn ze moeilijk te verwijderen. Dit is niet louter een schoonmaakkwestie, maar een probleem voor de patiëntveiligheid. Biofilms fungeren als reservoirs voor multiresistente micro-organismen (multi-drug resistant organisms – MDRO’s), waardoor ze worden beschermd tegen antimicrobiële middelen en tegelijkertijd de kans op horizontale genoverdracht toeneemt. Dit versnelt de verspreiding van resistentie.
Bacteriën in een biofilm zijn 10 tot 1.000 keer resistenter tegen antibiotica in vergelijking met hun planktonische tegenhangers.
Uit onderzoek blijkt dat tot 65% van alle microbiële infecties en zelfs 80% van de chronische infecties gerelateerd zijn aan biofilms. Biofilms kunnen leiden tot hardnekkige infecties, een toegenomen resistentie tegen behandelingen en een verhoogd risico op kruisbesmettingen. Hun aanwezigheid op medische apparatuur, oppervlakken en in omgevingen zoals watersystemen kan ook bijdragen aan ziekenhuisinfecties (HAI’s), wat een groot risico vormt voor de patiëntveiligheid.1,2
Zijn alle Biofilms hetzelfde?
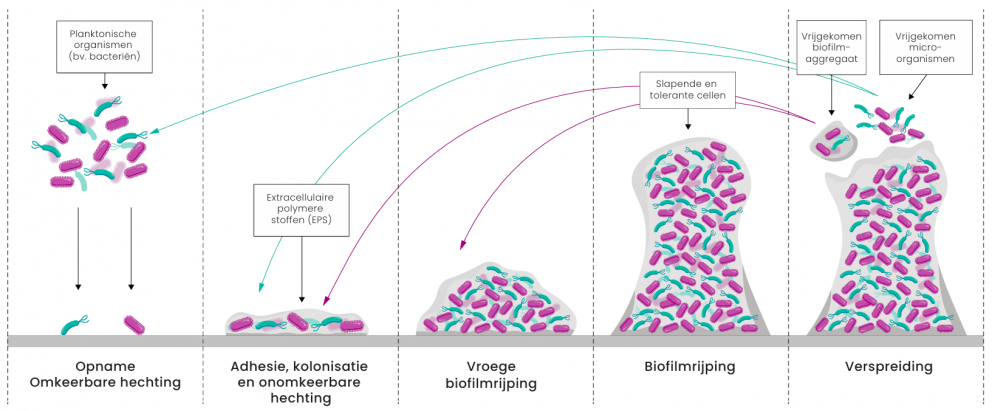
Hoewel alle biofilms bestaan uit een gemeenschap van micro-organismen die zijn ingekapseld in een beschermende matrix, kunnen hun samenstelling en eigenschappen variëren. Ze kunnen bestaan uit bacteriën, gisten en schimmels, en zelfs virussen. Ze bestaan doorgaans uit één of meer verschillende soorten organismen en kunnen vele uren op een oppervlak blijven zitten.
Natte biofilm wordt gevormd in vochtige omgevingen, waar micro-organismen goed kunnen groeien dankzij de aanwezigheid van water en voedingsstoffen. Deze micro-organismen scheiden een slijmerige laag extracellulaire polymere substantie (EPS) af, die polysacchariden, eiwitten en lipiden bevat, waardoor ze zich in een beschermende matrix nestelen. Meestal bestaan ze uit gramnegatieve bacteriën zoals Pseudomonas aeruginosa. In de gezondheidszorg kunnen natte biofilms zich ontwikkelen op en in de kanalen van herbruikbare medische hulpmiddelen, in waterleidingen en op wastafels, douches en toiletten en hun omliggende oppervlakken.
Droge biofilm bestaat uit micro-organismen die zich vormen in droge of vochtarme omgevingen met een tekort aan voedingsstoffen. Door deze barre omstandigheden zijn micro-organismen die ontwikkeld zijn in een droge biofilm doorgaans veerkrachtiger. In tegenstelling tot natte biofilms komen droge biofilms voor op oppervlakken met een minimale vochtigheid, zoals op medische apparatuur of droge oppervlakken in de omgeving. Deze biofilms zijn moeilijk op te sporen en te verwijderen, aangezien hun droge toestand zorgt voor een verhoogde weerstand tegen reinigings- en desinfectieprocedures.
Chloordioxide: een gerichte aanpak tegen Biofilms
Er bestaan methoden om na te gaan hoe effectief een desinfectiemiddel is tegen biofilms.
Voor natte biofilms kunnen de MBEC-test (ASTM E2799) en het CDC-model (ASTM E2871-22) worden gebruikt om de werking van desinfectiemiddelen tegen biofilms van Staphylococcus aureus en Pseudomonas aeruginosa te beoordelen.
Tristels chloordioxide is met deze methoden beoordeeld tegen biofilms die gedurende een periode van 72 uur werden gekweekt. Alle geteste chloordioxideoplossingen behaalden, bij hun respectieve contacttijden (van slechts 30 seconden), een reductie van ≥4 log in de MBEC-test en ≥5 log in het CDC-model. Deze snelle en krachtige werking is van cruciaal belang in de dagelijkse infectiepreventie‑ en controleprocessen (IPC), waar tijd en effectiviteit perfect op elkaar moeten aansluiten.
Voor droge biofilms werd de werking van chloordioxide beoordeeld met behulp van het CDC‑model (ASTM E2871‑22), aangepast met een dehydratie-/rehydratiecyclus van 12 dagen. Deze methode wordt steeds vaker erkend als representatief voor de reële uitdagingen bij decontaminatie van biofilms. Alle geteste chloordioxideoplossingen realiseerden een logreductie van ≥5 bij hun respectieve contacttijden.
Gevolgen voor Infectiepreventie
Aangezien chloordioxide effectief blijkt te zijn tegen zowel oppervlakteverontreinigingen als hardnekkige biofilms, zou de integratie ervan in routinematige IPC-protocollen kunnen helpen bij het aanpakken van het probleem van biofilms. Het zou ook de kloof kunnen overbruggen tussen naleving van de voorschriften en de daadwerkelijke effectiviteit ervan in de praktijk.
Onze high-level desinfectiemiddelen voor medische hulpmiddelen:
Onze sporicide desinfectiemiddelen voor oppervlakken in de gezondheidszorg:
Reference:
1 Ledwoch, K., Dancer, S.J., Otter, J.A., Kerr, K., Roposte, D., Rushton, L., Weiser, R., Mahenthiralingam, E., Muir, D.D. and Maillard, J.-Y. . (2018). Beware biofilm! Dry biofilms containing bacterial pathogens on multiple healthcare surfaces; a multi-centre study. Journal of Hospital Infection, 100(3), pp.e47–e56. doi:https://doi.org/10.1016/j.jhin.2018.06.028.
2 Maillard, J.-Y. and Centeleghe, I. (2023). How biofilm changes our understanding of cleaning and disinfection. Antimicrobial Resistance and Infection Control, [online] 12(1), p.95. doi:https://doi.org/10.1186/s13756-023-01290-4.
3 K Ledwoch, Vickery, K. and Maillard, J-Y. (2022). Dry surface biofilms: what you need to know. British journal of hospital medicine, 83(8), pp.1–3. doi:https://doi.org/10.12968/hmed.2022.0274.








